13,持つ持たれつ共有し。
第1族の元素と第7族の元素が結合している化合物はNaCl(塩化ナトリウム)のように
電子を1個失ったナトリウムイオンNa+(1価の陽イオン)と
電子を1個得た塩化物イオンCl − (1価の陰イオン)が1対1で結合しているが
第2族と第17族の元素が結合している化合物はCaCl2(塩化カルシウム)のように
電子を2個失ったカルシウムイオンCa2+(2価の陽イオン)1個と
電子を1個得たCl − イオン2個が結合している。
第2族と第16族の元素が結合している化合物はCaO(酸化カルシウム)のように
電子を2個失ったカルシウムイオンCa2+(2価の陽イオン)1個と
電子を2個得たO 2− (2価の陰イオン)1個が結合している。
第14族の炭素Cが他の原子と結合している場合はどうだろう。
C4+ なのか?、 C4− なのか?。
実は、第14族の炭素Cやケイ素Si はイオンになりにくいんだよ。
では第14族の元素はどんな結合をしているのだろう。
炭素Cと水素Hの化合物には天然ガスに含まれるメタンCH4は
1個の炭素Cに4個の水素が結合している。
炭素Cは最外殻に4個の電子があったね。
そこに4個の水素から得た電子を共有して
あたかも最外殻に8個の電子がある閉殻のようになっている。
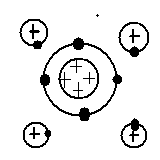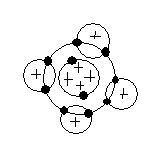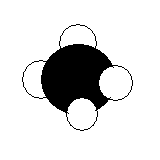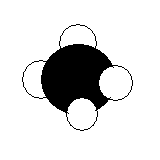 ←水素原子4個が炭素原子1個とくっつく。
←水素原子4個が炭素原子1個とくっつく。
水素Hの方はといえば、それぞれが炭素原子Cの電子を1個共有している。
すなわち、K殻に2個の電子を持つヘリウムHeと同じ閉殻の状態です。
多くの炭素化合物はこのような結合をしている。これを共有結合っていうんだ。
そこで問題だよ。
水晶は二酸化ケイ素SiO2といってケイ素Siと酸素Oが1:2で出来ている化合物だよ。
水晶はイオン結合でできているか、共有結合でできているか。
今日はここまで。じゃ、また、会おうよ(^0^`)
2006.1.2
*質問があったらここをクリック*
答え、共有結合
←もどる
◎
すすむ→
 ←水素原子4個が炭素原子1個とくっつく。
←水素原子4個が炭素原子1個とくっつく。